| 一、待测母液的制备 1. 原理:将硅酸盐岩石中的钾钠经钾经硫酸氢氟酸消化后,以硫酸盐形式而析出。 2. 试剂:①:1:1的硫酸(A.R) ②:40%氢氟酸(A.R) 3.方法:称取过140目筛并在105~110OC烘干试样0.5克(标准至0.0001克)于塑料王(或铂金)坩埚中,先用几滴水湿润后,加入1:1的H2SO4 0. 6~0.8毫升及40%HF14~20毫升,置于有调压器240OC左右的低温电炉上消化,并经常摇动坩埚,使试样作用分解完全。溶液蒸干后取出冷却,用热水脱取于100毫升烧杯中,将试液煮沸2~3分钟,冷却后定容100毫升,此待测母液可供测定Fe、Al、Ti、Ca、K、Na等元素用。 二、氧化钾的测定-季胺盐容量法 1.原理:钾离子与四苯硼钠作用,生成白色的四苯硼钾沉淀,此沉淀在碱性溶液中能定量地析出。过量的四苯硼钠在溴酚蓝指示剂存在下,用标准的溴化三甲基十六烷基铵(简称季胺盐,下同)进行滴定,溶液由紫红色变为纯蓝色即为终点。反应式如下: K++[B(C6H5)4]―→KB(C6H5)4↓[(CH3)3C16H33N]++[B(C6H5)4]―→(CH3)3C16H33N・B(C6H5)4↓ 若待测溶液中有NH4-干扰可加入中性甲醛,使之生成六次甲基四铵,消除干扰。 4NH4++6HCHO→(CH2)6N4+4H++6H2O 因瓷土中NH+4极少,可不必加入甲醛。Ca、Mg、Al、Fe等盐类与四苯硼钠不起反应,但因在碱性条件下进行滴定,上述离子生成氢氧化物沉淀,对四苯硼钠有吸附作用,可加入EDTA消除干扰,加入EDTA还能增加滴点的稳定性。此外,待测溶液的K2O含量应控制在0.5~1.6毫克范围,滴定体积应尽量相等,以便提高滴定的精度。 2.试剂: ① 20%NaOH(A.R) ② 0.1%溴酚蓝指示剂:称此试剂0.1克用少许水及2滴20%NaOH溶解后,再用水稀至100毫升贮于棕色瓶中备用。 ③ 0.05N四苯硼钠:称A.R的四苯硼钠1.8克溶于100毫升水中,加入氢氧化铝1.5克(也可加入1克AlCl3・6H2O代替),振荡10分钟,用密质滤纸过滤,如有浑浊,将滤液再倒回漏斗中反复过滤,过滤完毕后,滤液中加入20%NaOH4滴摇匀,贮于棕色瓶中备用。 ④ 0.025N季胺盐溶液:称本试剂1.8克,加200毫升水溶解后,用中速定性滤纸滤于塑料瓶中密封保存备用。 ⑤ 0。002123N:K2o标准溶液:称取在110OC烘干两小时的A.R氯化钾0.1583克(若按KCl含量99.8%计算,则应称KCl0.1586克),用水溶解后,定容1000毫升摇匀(此溶液即1毫升含钾K2O0.1毫克)。 3. 测定步骤: 吸取试样待测母液10.00毫升(含K2O1.0毫克左右),于100毫升三角瓶中,加10%EDTA1毫升左右,充分摇匀,一分钟后加入20%NaOH1.5~2毫升(PH值控制在12~13之间),摇匀后用吸管准确加入0.05N四苯硼钠1.00毫升,摇匀静置5分钟,加入0.1%溴酚蓝指示剂4滴,取3或5毫升微量滴定管,用0.025N标准季胺盐溶液滴定至纯蓝色一出现即为终点。记录季胺盐用量(若季胺盐用量过大,应调整试液容量,使季胺盐用量控制在0.5~1.5毫升左右)。 0. 025N季胺盐溶液的标定:吸取0.002123NK2O标准溶液10毫升(相当于1毫克K2O),于100毫升三角瓶中,加入10%EDTA1毫升摇匀,1分钟后,加入20%NaOH1毫升(PH值在12~13之间)摇匀,再准确加入0.05N四苯硼钠1.00毫升,滴定过程与试样相同,设滴定用去季胺盐Vs毫升。同时用10毫升水代替钾标准液,同样加入各种试剂,进行空白滴定,,设季胺盐用量为Vo毫升,则可以求出季胺盐的当量浓度:  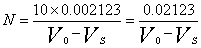 4. 结果计算(两次重复测定绝对相差<0.05%取平均值) 试样K2O%=  式中:V0-空白溶液滴定季胺盐用量(毫升); V样-试样溶液滴定季胺盐用量(毫升); N-季胺相加的标定当量浓度; 0.0471-1毫克当量的季胺盐相当于K2O的克数; 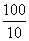 -待测液稀释倍数。 -待测液稀释倍数。 三、氧化 钠的测定 1. 原理 用Ba(OH)2调整试液酸度,分离Al3+、Fe3+、Ti4+、等干扰离子,再加过量的Ba(OH)2除去SO42-,最后通入CO2气体使Ca2+、Mg2+、Ba2+等离子成为碳酸盐沉淀过滤除去。碱金属以碳酸盐形式留在溶液中,用盐酸滴定钾、钠总量,扣除K2O,即为Na2O含量。 2,试剂: ① 5%Ba(OH)2溶液(A.R); ② 0.1%甲基红指示剂:称此试剂0.1克溶于90亳升无水乙醇中,再加入10毫升水; ③ 0.1%溴甲酚绿:称此试剂0.1克溶于50毫升无水乙醇中,加水至100毫升; ④ 0.1%酚酞:称酚酞0.1克溶于100毫升无水乙醇中; ⑤ 碳酸钠固体(A.R); ⑥ 二氧化碳气体:由气体发生器随制备随用; ⑦ 0.05NHCl标准液:量取21毫升浓盐酸用水稀释至5000毫升。 标定:称取在120oC烘干4小时的Na2CO3约0.05克(准确至0.0001克)于250毫升烧杯中,加水100毫升煮沸,加8滴甲基红指示剂及13滴溴甲酚绿指示剂,用0.05NHCl标准液滴定至溶液由蓝绿色变为暗红色即为终点。即可求HCl的当量浓度: NHcl=  式中:W-称取Na2CO3重量(克) V-滴定时消耗的HCl量(毫升); 0.05299-Na2CO3的毫克当量。 3.测定步骤: 吸取待测母液25.00亳升,加水75毫升加热煮沸30分钟,加8滴甲基红指示剂。边加入5%Ba(OH)边搅拌,至试液变黄色(PH6.2)再过量2-3滴(pH=7左右),煮沸后取下趁热用中速定性滤纸过滤,热水洗5-6次滤纸后弃去沉淀。将液浓缩至100毫升左右,在不断搅拌下,慢慢加入5%Ba(OH)210毫升,继续煮沸5分钟,冷至室温,加入酚酞指示剂1滴,通入CO2使试剂由红色变为黄色,再通气一分钟,把试液移至电炉上浓缩至30~40毫升左右,用中速定性滤纸过滤,用冷水洗几次烧杯漏斗,使总体积在70~80毫升左右,煮沸,加13滴溴甲酚绿指示剂,用0.05NHCl标准液滴定至暗红色即为终点。 4.结果计算; 先把碱性氧化物(R2O)含量全部换算成K2O含量(两次重复测定绝对相差<0.05%取平均值): R2O%=  Na2O%= 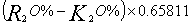 式中:N-HCl当量浓度; V-滴定时消耗HCl量(毫升); 0.0471-1毫克当量的盐酸相当于K2O的克数; 0. 65811- 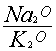 的比值; 的比值; K2O%-用季胺盐测定数K2O百分含量; G-烘干样量(克)。 季胺盐容量法火焰光度法测定钾比较 试样编号 | 火焰光度法测得样K(%) | 季胺盐容量法测得试样K(%) | 两次重复测定值 | 平均值 | 两次重复测定值 | 平均值 | 17-1 17-2 | 1.07 1.12 | 1.10 | 1.14 1.09 | 1.12 | 18-1 18-2 | 0.97 1.02 | 1.00 | 1.01 0.99 | 1.00 | 19-1 19-2 | 1.29 1.25 | 1.27 | 1.30 1.26 | 1.28 |
季胺盐容量法对纯钾盐(KCl)中钾的回收率测定 加入K的毫克数 | 加入四苯硼钠量(毫升) | 测定季胺盐用量(毫升) | 季胺盐当量浓度(N) | 1毫升季胺盐相当四苯硼钠毫升数 | 测得K的毫克数 | K的回收率(%) | 误差(毫克) | 空白(蒸馏水) 空白(蒸馏水) | 1 1 | 0.84 0.88 | 0.04442 | 1.16 | | | | 1.175 1.175 | 2 2 | 1.04 1.05 | 0.04442 | 1.16 | 1.179 1.168 | 100.3 99.4 | +0.004 +0.007 | 2.35 2.35 | 2 2 | 0.38 0.37 | 0.04442 | 1.16 | 2.329 2.346 | 99.1 99.8 | -0.021 -0.004 | 4.70 4.70 | 5 5 | 1.52 1.48 | 0.04442 | 1.16 | 4.833 4.947 | 102.8 105.3 | +0.133 +0.247 |
|

